医科2021.10.16 講演
[保険診療のてびき]
アルツハイマー病の早期診断について -最近の話題-(2021年10月16日)
兵庫医科大学 脳神経内科教授 武田 正中先生講演
はじめに
厚生労働省老健局の発表(2019年)によると、わが国の認知症高齢者数は462万人にのぼり、2025年には675万人から730万人に達すると推計されている。高齢者の約4人に1人は認知症もしくは軽度認知障害(MCI)で、7人に1人は認知症との計算になる。さらに、その患者数は今後も急速に増加することが予想される。認知症の原因疾患としてアルツハイマー病(AD)はその5~7割を占めるとされ、早期ADの診断法および疾患修飾薬(根本的治療薬)の開発は喫緊の課題である。これまでは、ADの臨床診断や薬剤臨床試験の効果判定には、認知機能尺度や日常生活(ADL)尺度が用いられてきたが、これらはADの病態を直接反映するものとは言い難かった。臨床試験でのADに対する疾患修飾薬の適応および効果判定を、効率的かつ正確に判定するには、ADの早期診断と効果判定を正確にすることが必須である。そのためには、従来使用されてきた認知機能尺度やADL尺度に代わり、ADの病態そのものを客観的および定量的な検出が可能なバイオマーカーの開発が必要である。
AD治療の研究は、現在は抗アミロイドβ療法が主体であり、早期AD、MCIやpreclinical ADへと対象がシフトしている。この疾患修飾薬である抗アミロイドβ療法が使用可能になった時には、治療標的分子であるアミロイドβの存在を確認する検査が必要になる。ADの早期診断について解説し、そのバイオマーカーについて最近の知見を共有する。
ADの病態およびバイオマーカーの時系列変化
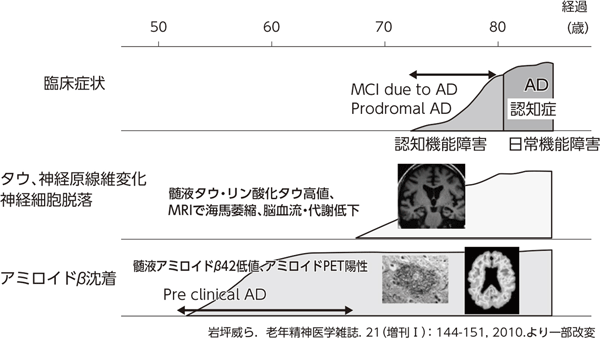
80歳でAD認知症を発症する場合、脳内病変はその約25年前から始まっているとされる(図)。最初に出現するのはアミロイドβの沈着で、これは脳脊髄液アミロイドβ42の低下あるいはアミロイドPETによって検出できる。続いてタウによる脳神経細胞傷害が出現し、海馬萎縮や側頭葉および頭頂葉の代謝・血流の低下、そして記憶障害や認知機能障害が出現する。2011年NIA/AAによる改定診断基準では、認知機能障害は認めないが、脳内にAD病理変化が認められる時期をpreclinical ADとし、バイオマーカーで診断するとしている。さらに、2018年NIA/AAによる臨床試験の診断基準で、アミロイドβ蓄積(A)、リン酸化タウ蓄積(T)と神経変性・損傷(N)の3段階に分けて診断することを提唱している。
このように、認知症・軽度認知障害は臨床症状によって定義されるが、その原因となるADは臨床症状ではなく病理診断かバイオマーカーで定義される。
体液バイオマーカー
現在、ADの診断のための体液バイオマーカーは、髄液リン酸化タウ値のみが保険適用である。今後、疾患修飾薬が可能となった場合、ADの早期診断および病態進展の診断に有用な体液バイオマーカーの測定が重要になると思われる。ADの診断バイオマーカーは、特徴的な病理的変化である老人斑と神経原線維変化を構成するアミロイドβタンパクとタウタンパクが最も重要である。体液バイオマーカーでは、髄液アミロイドβ42の低下、総タウ値およびリン酸化タウ値の上昇がADの診断マーカーとして推奨される。また髄液と比較して、血液マーカーは侵襲が低く汎用性があり、開発が進んでいる。少量の血液からアミロイドベータを測定できる機器も研究が進んできており、これからはまず血液でふるい分け、疑いのある患者にアミロイドPETを行うといったより効率的な方法がなされていくと期待される。
アミロイドPETの有用性について
新しい治療戦略(疾患修飾薬)においては、ADの早期発見が重要である。臨床症状のみでは、病理の種類や予後の予想は困難である。現在の日常診療にはMRIと脳血流SPECTが用いられている。アミロイドPET検査は、ADの早期診断の検討で、ADに転向したMCI患者では、非転向MCI患者に比べPiB保持率が高いとする多くの研究がある。よって、従来の画像検査に11C-PiB PETを追加することによって、MCIがAD認知症にコンバートする可能性を予測し、早期に治療を開始することができる可能性がある。
ADの新しい治療
現在のADの認知症に対する薬物治療では、保険適用はコリンエステラーゼ阻害薬3薬剤とNMDA受容体拮抗薬1薬剤である。しかしながら、これらの薬は効果が限定的で、根本的薬物治療が待ち望まれている。2021年6月にADの新薬を、アメリカの食品医薬品局(FDA)は治療薬として承認した。このADの新薬アデュカヌマブはアミロイドβを取り除き、神経細胞が壊れるのを防ぐとしている。1年半の投与でアミロイドベータが59~71%減少したとの報告がある。この薬は病気の上流の過程で、原因、すなわち病気のメカニズムに直接働きかけて改善しようというもので、MCIと軽症の認知症の段階を対象にしている。
アミロイドPETが臨床研究や治験で使えるようになってきたため、アミロイドβがない認知症患者を除外して正確な治験ができ、薬の効果も測りやすくなった。日本でも昨年12月に承認申請された。同じような効能をもつレカネマブ、ガンテネルマブやドナネマブなどの治験結果も徐々に出てきている。ドナネマブではタウタンパク質の減少も示されており、さまざまな段階の方に適用できる治療法も進むことが期待されている。
(2021年10月16日、第42回神戸支部総会記念講演より)
1)岩坪威ら.老年精神医学雑誌.21(増刊Ⅰ):144-151, 2010.
2)McKhann GM. et al. Alzheimers Dement. 7:263-269, 2011.
3)Jack CR Jr. et al. Alzheimers Dement 14:535-562, 2018.
4)Grimmer T. et al. J Nucl Med. 57:204-207, 2016.
5)Kikukawa T. et al. Neurol Sci. 39:1597-1602, 2018.
図 ADの臨床経過と神経細胞・アミロイドβ病理