医科2022.04.16 講演
[保険診療のてびき]
歯周病菌による炎症と認知症最前線
-医歯連携で認知症予防を実現へ-
(2022年4月16日)
九州大学大学院歯学研究院 口腔機能分子科学分野OBT研究センター准教授
はじめに
高齢人口の増加に伴い、全世界の認知症患者数は2050年には1億5千万人を超えると推測される。アルツハイマー型認知症(Alzheimer's disease, AD)は認知症の7割を占め、ADの脳病態にはアミロイドβ(Aβ)蓄積と神経原線維変性に加え、ミクログリアに依存した脳内炎症があり、全身炎症は脳内炎症を誘発し、ADの発症や進行を促進する1)。歯周病は中高年の8割に発症し、歯周病菌のP.gingivalisの成分がAD脳に検出されることから、ADへの関与が注目されている。私たちは歯周病を慢性炎症と捉え、歯周病菌であるP.gingivalis菌のADへの関与メカニズムを解明し続けている。
本講演ではP.gingivalis菌のADへの関与について、私たちが得られた知見を踏まえて解説し、全身炎症への介入による、認知機能の改善効果も紹介する。
P.gingivalisのADへの関与メカニズム
1.P.gingivalisがAD脳病態を誘発し促進するP.gingivalis(P.g)LPSの全身曝露は野生型中年マウスに記憶障害、脳内ミクログリア活性化ならびにニューロン内Aβ産生といったAD様脳病態を誘発した。一方、P.gLPSを投与したリソソーム酵素のカテプシンB(CatB)欠損マウスではAD様脳病態は生じなかった。
またP.gLPSは脳から単離したミクログリアにCatBに依存したIL-1βの産生を増大した。さらにP.gLPSで刺激したミクログリア培養上清(MCM)は初代培養ニューロンにおいて、Aβ産生を誘導し、そのAβがCatBを特異的阻害したMCMにより抑制された。
これらの結果からPgLPSはミクログリアのCatBを介して、ニューロン内Aβ産生を誘導し、記憶低下をもたらすことがわかった2)。
2.P.gingivalisが全身炎症を増大させる
P.gLPSの全身曝露により、野生型中年マウスの肥大させた脾臓に樹状細胞とTh17細胞が増加し、カテプシンS(CatS)ならびにIL-6が増えた。しかしP.gLPSを投与したCatS欠損マウスでは脾臓に炎症は増大しない。
さらにP.gLPSは脾臓から単離した樹状細胞のIL-6を増加させ、その産生はCatSを特異的阻害により抑制した。
IL-6とTh17とも炎症促進因子であることから、P.gLPSはCatSに依存した脾臓に炎症を増大させることが明らかになった3)。
一方P.gingivalis菌の全身感染では中年マウスの肝臓にあるマクロファージにIL-1βが増え、P.gingivalis菌は肝臓に炎症を増大させることも分かった4)。
3.P.gingivalisが脳外でAβ産生を誘導する
AD脳におけるAβは脳で作られると考えられている。私たちは世界で初めて慢性歯周病患者の歯肉において、AβがIL-1βを産生する炎症性マクロファージを発見した。またP.gingivalis菌に全身感染した中年マウスの肝臓における炎症性マクロファージにもAβが発見された。貪食機能をもつマクロファージが血液中のAβを取り込む可能を否定できないため、P.gingivalisを直接培養マクロファージに感染させることにした。
驚いたことに、P.gingivalisは培養マクロファージにAβ産生を誘導し、CatBの特異的阻害によって、そのAβ誘導が抑制された。P.gingivalisは脳外の炎症組織において、CatBに依存したAβを誘導することが明らかになった4)。
4.P.gingivalisが脳外のAβを脳内に輸送させる
P.gingivalisによる脳外で産生されるAβが脳内に輸送される可能性について、血液脳関門(blood-brain barrier、BBB)構成の脳血管内皮細胞における糖化最終産物の受容体(receptor for advanced glycation end product, RAGE)に着目した。
P.gingivalisに3週間感染した中年マウスは脳血管内皮細胞におけるRAGEは2倍に、その周囲脳実質内のAβが10倍に増えた。BBB機能モデルのhCMEC/D3細胞を用いて検討した結果、P.gingivalisはhCMEC/D3細胞にNFκB活性化に依存したRAGEを増やし、hCMEC/D3を通過するAβ量を16倍に増加させ、RAGE特異的阻害はP.gingivalisにより、Aβ量を60%に減少させた。
よってP.gingivalisはCatB/NFκBに依存したRAGE増加を介して、Aβの脳内へ輸入を促進することが明らかになった5)。
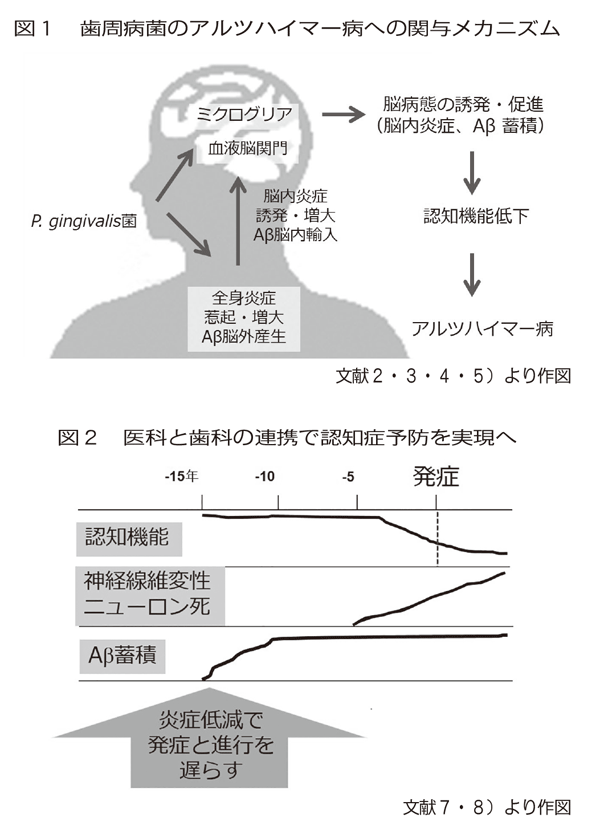
これまでの研究結果から、歯周病に伴う全身をめぐるP.gingivalisとその成分が多方向にADの発症と進行に関与することが明らかになっている(図1)。
全身炎症の介入によりヒト認知機能の改善
高齢につれてADリスクが上昇し、加齢に伴う炎症促進因子と炎症抑制因子のバランス崩れによって増大する全身炎症はその一因と考えられる6)。私たちがチベット高原に在住する高齢者を対象に行った2年間の介入研究で、高齢者の血清中IL-1β、IL-6、TNF-α(炎症促進因子)の増加とTGF-β1(炎症抑制因子)の低下によって、全身炎症が増大され、それに伴い認知機能が大幅に低下した。
一方サプリメント(プロポリス)を経口服用した高齢者の血清中TGF-β1の増加とIL-1β,IL-6,TNF-αの低下による全身炎症が軽減され、認知機能が低下しなかった。この研究は慢性全身炎症の軽減が認知機能低下を防ぐ可能性を実証した7)。
ADはAβが脳に蓄積してから25年ほど後に発症する、長いスパンで進行する病気であり8)、全身炎症と脳内炎症はその上流に位置することが示唆されている。
認知症の7割を占めるADは発症してからの根本的な治療法がまだ開発されていない現状の中、認知症の現実的な対策として、医科と歯科の連携で、炎症制御が大いに期待される(図2)。
参考文献
1)McGeer EG McGeer PL. J Alzheimers Dis. 19:355-361. 2010.
2)Wu Z. et al. Brain Behav Immun. 65:350-361, 2017.
3)Dekita M. et al., Front Pharmacol. 8: 470. 2017.
4)Nie R. et al. Alzheimer's Dis.72: 479-494. 2019.
5)Zeng F. et al., J Neurochem.158: 724-736. 2021.
6)Holmes C. et al., Neurology. 73:768-774. 2009.
7)Zhu A. et. al. J Alzheimers Dis. 63: 551-56. 2018.
8)Bateman RJ. N. Eng. J. Med. 367: 795-804. 2012.
(4月16日、神戸支部研究会より)